En la naturaleza son muy abundantes los compuestos con ciclos de cinco y seis eslabones. Sin embargo, los ciclos de tres y cuatro miembros aparecen muy rara vez en productos naturales.
Estabilidad en cicloalcanos
Estos hechos experimentales sugieren la mayor estabilidad de los ciclos de cinco o seis miembros con respecto a los de tres o cuatro.
En el año 1885, el químico alemán Adolf von Baeyer propuso que la inestabilidad de los ciclos pequeños era debida a la tensión de los ángulos de enlace. Los carbonos sp3 tienen unos ángulos de enlace naturales de 109,5º, en el ciclopropano estos ángulos son de 60º, lo que supone una desviación de 49,5º. Esta desviación se traduce en tensión, que provoca inestabilidad en la molécula.
El ciclobutano es más estable puesto que sus ángulos de enlace son de 90º y la desviación es de sólo 19,5º. Baeyer aplicó este razonamiento al resto de cicloalcanos y predijo que el ciclopentano debería ser más estable que el ciclohexano.
Tensión angular
Obsérvense los ángulos de enlace de los diferentes cicloalcanos:
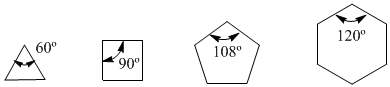
Como el ángulo natural de un carbono sp3 es de 109,5º, von Baeyer razonó que el cicloalcano más estable era el ciclopentano. Si embargo, sabemos que Baeyer estaba equivocado ya que el cicloalcano de menor energía (más estable) es el ciclohexano. El error de Bayer está en suponer que los cicloalcanos son planos y que el único tipo de tensión que presentan es debido a los ángulos de enlace.
Tipos de tensión anular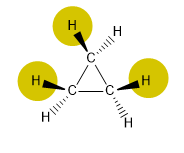
Existen tres tipos de tensión que desestabilizan los compuestos cíclicos:
1.- La tensión del ángulo de enlace, debida a ángulos que difieren de los 109,5º.2.- Tensión de eclipsamiento, debida a átomos o grupos de átomos próximos, que sufren repulsiones (tensión estérica).
El ciclopropano presenta una tensión muy importante, debida a los bajos ángulos de enlace y a las interacciónes entre hidrógenos (eclipsamientos)









