Se llaman conformaciones a las diferentes disposiciones espaciales que puede adoptar una molécula y que se interconvierten a temperatura ambiente por rotación
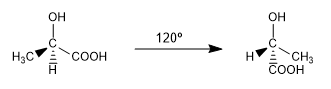
Son dos de las infinitas conformaciones que se pueden dibujar del ác. 2-hidroxipropanoico. A temperatura ambiente la molécula está girando continuamente pasando por todas las posibles conformaciones.
Ahora veamos las dos conformaciones más características del etano, la conformación alternada y la eclipsada.
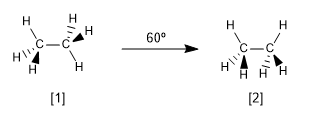
[1 ] Conformación alternada del etano
[2 ] Conformación eclipsada del etano
Algunas reacciones son muy dependientes de la conformación en la que se dispone la molécula. Así la eliminación E2 requiere que las moléculas adopten la disposción ANTI y su velocidad es dependiente de la concentración de moléculas que se encuentran en esta conformación.
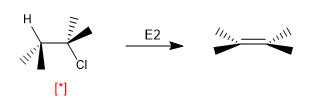
[*] Disposición "ANTI" H-Cl
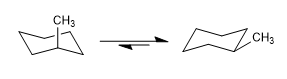
Los ciclohexanos también presentan dos conformaciones de silla que se interconvierten a temperatura ambiente. La conformación que deja más grupos en la posición ecuatorial suele ser la de mayor estabilidad.
Otro ejemplo de equilibrio conformacional lo presentan los bifenilos. Cuando ambos anillos se disponen en el mismo plano forman un sistema aromático, el giro de 90º romple la conjugación entre ambos y vuelve la molécula más inestable.
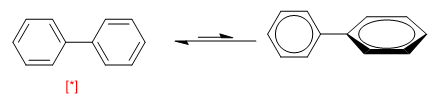
[*] Conformación más estable
Sin embargo, la presencia de grupos voluminosos en las posiciones orto respecto de ambos anillos produce repulsiones que obligan a la molécula a girar, siendo en este caso más estable la conformación con los anillos perpendiculares.
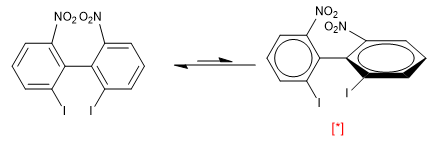
[*] Conformación más estable
A temperatura ambiente solo se observa la conformación más estable (lado derecho). La repulsión entre los dos nitros y los dos yodos es tan importante, que la rotación del bifenilo tiene una energía de activación de 19 Kca/mol.
Algunos enlaces, aunque aparentemente son simples, no permiten el libre giro de los grupos en torno a ellos. Los metilos de la DMF dan dos singuletes, a distinto desplazamiento químico, en el espectro de RMN debido a que el enlace C-N tiene un importante carácter de doble enlace y restringe la rotación de los grupos.
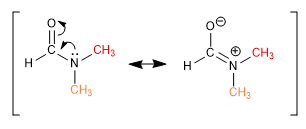
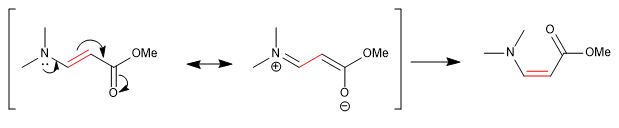
Otros enlaces, que aparentemete son dobles, permiten la rotación debido a la contribución de una estructura resonante en la que se comportan como enlaces simples.