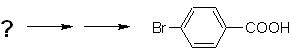SINTESIS SENYAWA AROMATIK I
(Metode Pohon Sintesis)
Usulkan rencana sintesis, menggunakan toluena atau xilena sebagai bahan awal, untuk molekul-molekul berikut:
(MOb 12)
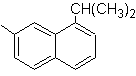
1-isopropil-7-metilnaftalena | (MOb 13)
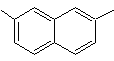
2,7-dimetilnaftalena |
(MOb 14)
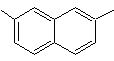
1-isopropil-6-metilnaftalena | (MOb 15)
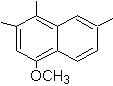
4-metoks-1,2,7-trimetilnaftalena |
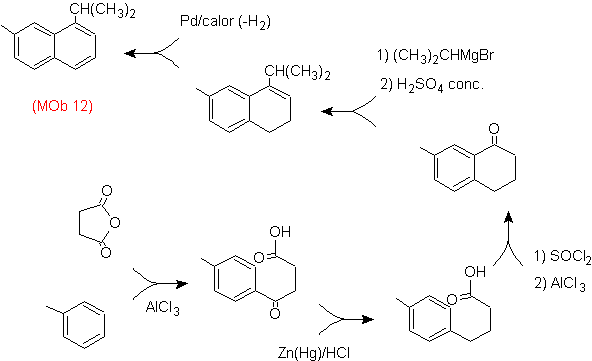
Solusi: (MOb 12).
Dalam strategi yang diasumsikan, diperhitungkan bahwa tahap terakhir dapat merespons proses "aromatisasi", yang diusulkan agar molekul prekursor menghadirkan cincin non-aromatik, dengan ikatan rangkap.
pada karbon yang mengandung ikatan rangkap dan gugus alkil.
Struktur ini dapat dicapai dengan aksi Grignard pada karbonil dan dehidrasi selanjutnya dari alkohol yang terbentuk. Keton dibentuk oleh asilasi pada senyawa benzena yang sesuai dengan anhidrida suksinat dan penutupan asilasi intramolekul Friedel-Crafts berikutnya.
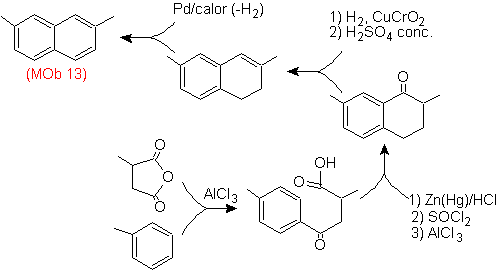
Solusi (MOb 13).
Sekali lagi, molekul prekursor harus "diaromatisasi", strategi yang paling tepat di antara yang lain Ini didasarkan pada kombinasi asilasi dengan anhidrida suksinat tersubstitusi dan reduksi Clemmensen.
Karbonil terakhir direduksi menjadi alkohol yang kemudian akan didehidrasi dengan molekul hidrogen dan katalis yang disebut kromil tembaga.
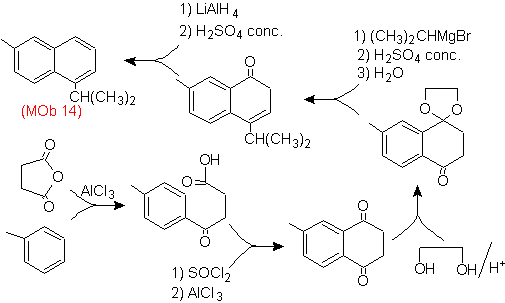
Solusi (MOb 14).
Aromatisasi akhir dicapai setelah mereduksi gugus karbonil menjadi alkohol dan kemudian mendehidrasinya. Molekul prekursor diperoleh dengan asilasi dengan anhidrida suksinat.
Karbonil yang harus diserang oleh Grignard untuk memasukkan gugus alkil dan menghasilkan alkohol yang akan didehidrasi, untuk sementara dilindungi sebagai asetal siklik.
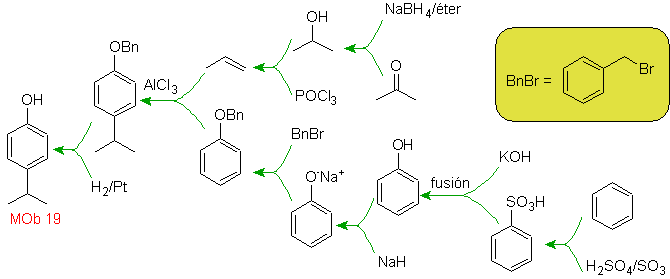
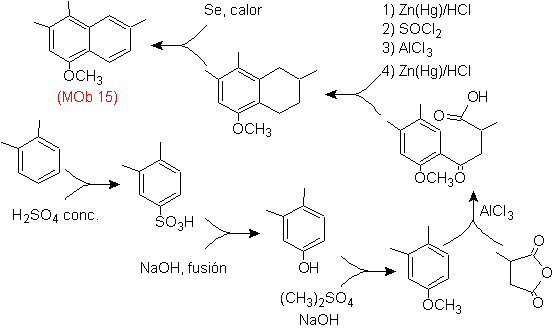
Solusi Mob 15 .
Cincin yang paling tersubstitusi dianggap sesuai dengan cincin aromatik yang melalui asilasi cocok dengan turunan suksinat anhidrida, ini akan memungkinkan penutupan cincin, dengan kombinasi asilasi dan reduksi karbonil yang cerdas.
Cincin benzena dengan fungsionalitas yang diperlukan dibuat dari o-xilena, yang disulfonasi dan gugus –OH dilindungi dengan eterifikasi sampai akhir.
Asilasi naftalena tunduk pada efek pelarut yang menarik. Reaksi dalam karbon disulfida atau pelarut terhalogenasi menghasilkan serangan terutama pada posisi a , namun, dalam larutan nitrobenzena, ukuran agen penyerang elektrofilik meningkat dengan solvasi dengan nitrobenzena, menyerang posisi b , yang kurang terhambat secara sterik.
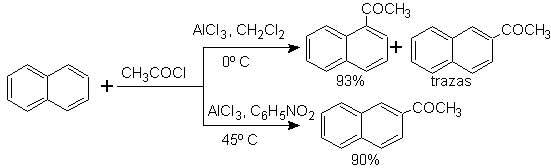
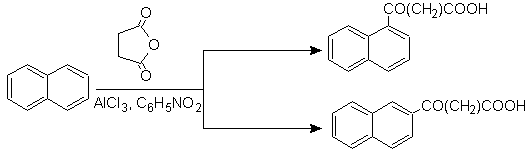
Suksinoylasi naftalena menjadi nitrobenzena menghasilkan campuran isomer a dan b yang dapat dipisahkan , keduanya digunakan dalam sintesis turunan fenantrena.
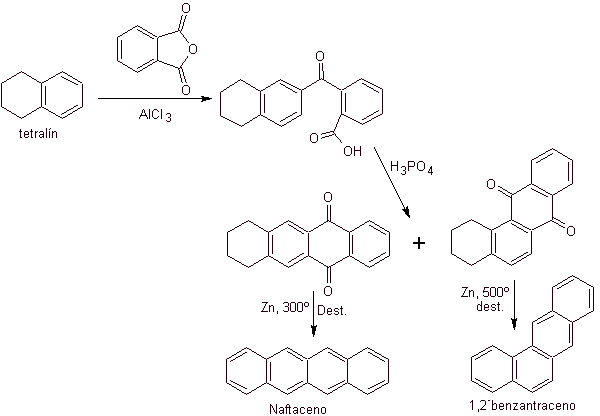
Tetralin diasilasi secara eksklusif pada posisi- b , menunjukkan ketahanan turunan 2-phthaloyl terhadap siklisasi pada posisi-3 untuk menghasilkan kondensat linier.
Contoh: Mensintesis asam p -bromobenzoat dari benzena dan reagen yang diperlukan. |
MOb 16 |
Solusi (MOb 16).
Perlu ditanyakan "Apa prekursor langsung asam p-bromobenzoat?" Analisis retrosintetik dari
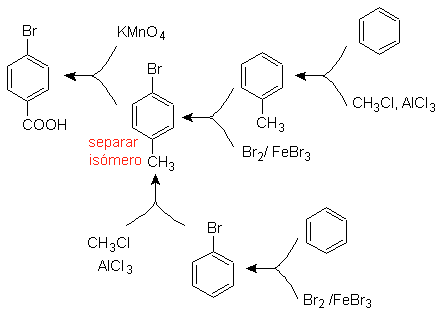
Pilihan terbaik adalah yang menggunakan toluena sebagai perantara, karena gugus metil mengaktifkan cincin benzena dengan lemah dan meningkatkan hasil pembentukan p-bromotoluena.
Pada jalur sintesis kedua, harus diperhitungkan bahwa bromin adalah penonaktifan cincin, dan oleh karena itu hasil reaksi jelas akan jauh lebih rendah daripada jalur pertama. Namun, harus dipahami bahwa tidak ada satu pun produk dalam sintesis, karena isomer tersubstitusi orto juga akan terbentuk, yang harus dipisahkan dalam proses sintesis.
Kasus kedua, yang menunjukkan karakteristik multisubstitusi elektrofilik dari cincin benzena, adalah sintesis 4-kloro-1-nitro-2-propilbenzena (MOb.17) dari benzena.
Solusi (MOb 17).
Pada prinsipnya ada tiga kemungkinan prekursor tersubstitusi, tetapi hanya satu yang cocok. Juga dalam hal ini, ada kemungkinan besar pembentukan isomer 2-kloro-1-nitro-4-propilbenzena.
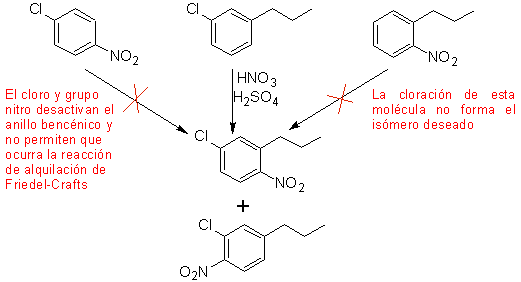
sintesis akhir dari
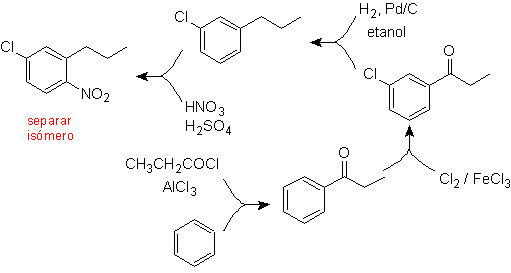
Sekarang jelas bahwa salah satu tugas ahli kimia adalah merancang jalur sintesis yang sejauh mungkin mengarah pada pembentukan produk tunggal dengan hasil tertinggi, yaitu menghindari pembentukan isomer di seluruh proses. Untuk mencontohkan aspek ini, kita akan mempelajari sintesis molekul-molekul berikut:
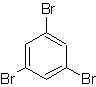
Massa. 18
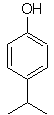
| Massa. 19
|
Solusi MOb 18
Brom berorientasi orto ke dan juga menonaktifkan cincin benzena, sehingga resor strategi untuk menempatkan gugus pengaktif yang kuat pada posisi orto dan para dari elektrofil baru dan setelah menghasilkan reaksi, menghilangkan gugus pengaktif dari cincin benzena.
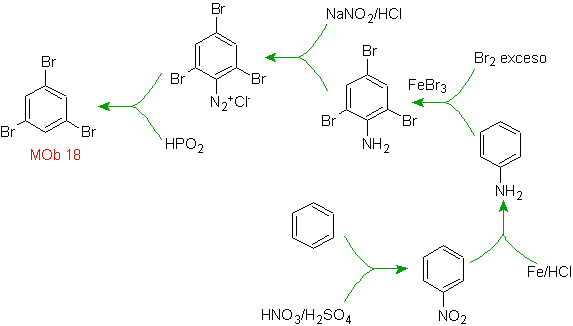
Gugus –OH adalah aktivator kuat dari cincin benzena dan orientasi orto-para. Akibatnya, kita dapat mengubah gugus –OH menjadi gugus yang jauh lebih besar, yaitu, besar, yang akan memberikan penghalang sterik untuk setiap elektrofil yang mendekati cincin dan hanya akan mengarahkannya ke posisi para. Akhirnya, gugus –OH akan dipulihkan, untuk mencapai molekul target.