Síntesis de anestésicos locales
derivados del ácido benzoico
|
Las propiedades de los alcaloides aislados de las hojas de
la planta de coca, fueron descubiertas por vez primera por Gaediche
en 1855, la purificación y aislamiento del principio activo denominado
cocaína por Albert Nieman en 1860, prácticamente dio inició a la historia
de los anestésicos locales. Posteriormente, Einhorn introdujo en
1904 la procaína (novocaína) como anestésico local en la medicina. |
|
A partir
de entonces, la humanidad ha asistido a un desarrollo continuo y sostenido de
la síntesis de nuevas moléculas con principios activos anestésicos:
![]() En 1925 Niescher sintetizó la nupercaína.
En 1925 Niescher sintetizó la nupercaína.
![]() En 1928 Von Eisleb la tetracaína
(pantocaína) y
En 1928 Von Eisleb la tetracaína
(pantocaína) y
![]() En 1946 Lofgren y Lundquist sintetizaron la
lognicaína (xylocaína o lidocaina)
En 1946 Lofgren y Lundquist sintetizaron la
lognicaína (xylocaína o lidocaina)
![]() Luego en 1954 Af Ekenstam y Egner
obtuvieron la síntesis de la mepivacaína (scandicaína).
Luego en 1954 Af Ekenstam y Egner
obtuvieron la síntesis de la mepivacaína (scandicaína).
![]() Posteriormente en 1960 y 1964 se
introdujeron en
Posteriormente en 1960 y 1964 se
introdujeron en
![]() Por último, los siguientes años han sido
incorporados nuevos anestésicos a la medicina
Por último, los siguientes años han sido
incorporados nuevos anestésicos a la medicina
Los anestésicos
locales, son los fármacos que al ser aplicados en alguna determinada zona
del organismo, producen en la misma la pérdida temporal y reversible de la
sensibilidad (térmica, dolorosa y tactíl), sin inhibición de la conciencia del
paciente. El tiempo de duración del
efecto del fármaco depende de la dosis utilizada, de su estructura química, de
la formulación y de la forma farmacéutica del medicamento.
En general, los fármacos anestésicos locales
responden a diferentes estructuras químicas, pero todos ellos con efectos
similares o intensidades diferentes del efecto anestésico. Sin embargo se puede
hacer un intento de agruparlos en esteres del ácido benzoico, esteres del ácido
aminobenzoico, Amidas, etc.
1. Estructura química de los anestésicos locales
Loa
anestésicos locales, predominantemente son bases débiles y están formados por
un grupo areno, éster o amida, que le
confiere a la molécula propiedades lipofílicas (que determinan principalmente
la potencia del fármaco), un grupo amino terciario alifático (alquílico o
alicíclico), que proporciona a la molécula su carácter hidrofílico y una cadena
intermedia alquílica que une las partes del areno con la amina y es la
responsable del nivel de toxicidad del
fármaco.
Así,
los principales anestésicos locales utilizados en las diferentes disciplinas
médicas, se pueden encontrar en los siguientes grupos:
a)
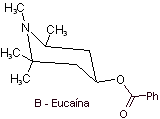
Ésteres amínicos del acido benzoico:
b)
Esteres del ácido m-aminobenzoico:
c)
Esteres del ácido p-aminobenzoico:
d) Amidas:
e)
Cetonas:
f)
Otros grupos
2. Síntesis de Anestésicos locales derivados de ésteres amínicos
del ácido benzoico
Los
fármacos más representativos de este grupo, son la cocaina, hexilcaína,
piperocaína, aminobenzoato de etilo, meprilcaína, amilocaína, ciclometicaína y
propanocaína. Estos nombres responden a
A
continuación se expondrán la síntesis en detalle de varios de ellos, a modo de
ejemplo de la aplicación de la metodología de síntesis, conocida como el método
de las desconexiones o del sintón, El orden de exposición no tiene
ninguna relación sobre la mayor o menor importancia de los mismos, puesto que
el objetivo que se busca, es adentrarse sobre el estudio de la síntesis química
de estos fármacos. Existen tratados
especializados de la farmacocinética y farmacodinámica de estas moléculas.
|
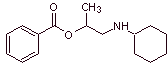
MOb 01: El clorhidrato de Hexilcaína, también
llamado ciclaína (Merck) u osmocaína, es un anestésico local de acción corta.
Proponer un diseño de síntesis, a
partir de materiales simples y asequibles, para este fármaco. |
|
Análisis retrosintético: La presencia de la amina secundaria en la estructura de
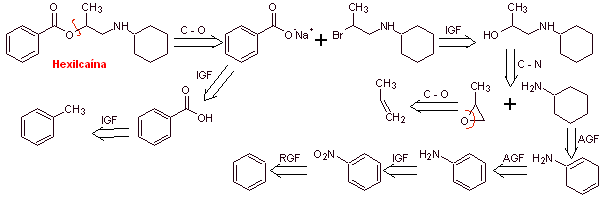
Síntesis de la hexilcaína: El aminoalcohol requerido como
intermediario, se prepara por la apertura del epóxido adecuado con la amina
(nucleófila) primaria correspondiente.
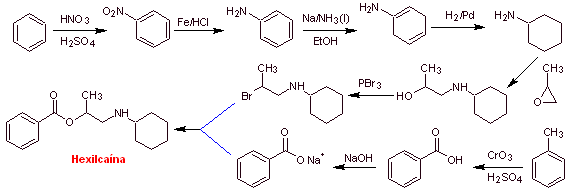
|
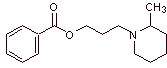
MOb 02. La piperocaína es un fármaco anestésico local utilizado como su sal de
hidrocloruro. Proponer un plan de síntesis para este fármaco. |
|
Análisis
retrosintético: La estructura de
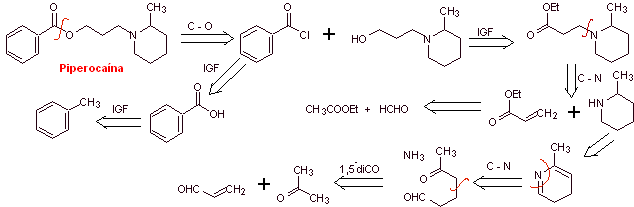
Síntesis de
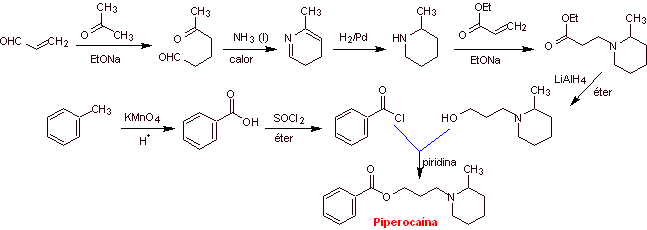
|
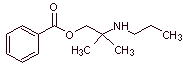
MOb 03: La meprilcaína, conocida
también como epirocaína, es un
anestésico local, de duración moderada. Proponer un diseño de síntesis para
esta molécula a partir de materiales simples y asequibles. |
|
Análisis retrosintético: La estructura de
Luego
se continúa con la desconexión de las dos moléculas precursoras, se desconecta
el enlace C-N de la amida y se continúa esta operación hasta llegar al acetato
de tilo y tolueno como materiales de partida.
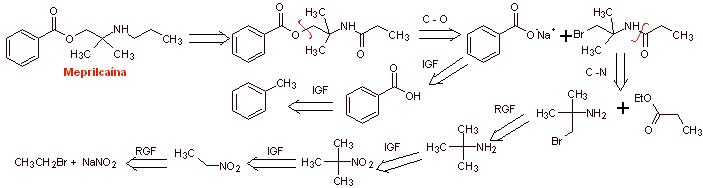
Síntesis de
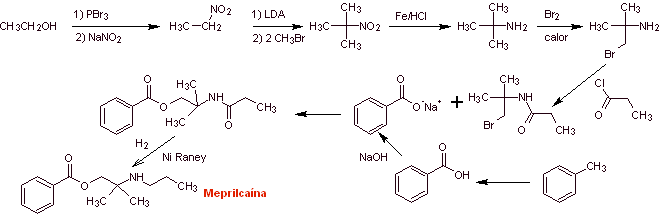
|
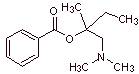
MOb 04: La amilocaína fue el primer
anestésico local sintético patentado por Ernest Fourneau Stovaine (francés)
en el Instituto Pasteur en 1903. Proponer un diseño de síntesis para esta
molécula, a partir de materiales simples y asequibles |
|
Análisis retrosintético: El proceso de desconexión se
inicia por en lace acilo-oxígeno, la posterior desconexión del enlace N-C del
amino alcohol, descubre la estructura de un epóxido sustituido y la
dimetilamina como moléculas precursoras. El epóxido puede formarse a partir de
una cetona con iluro de azufre.
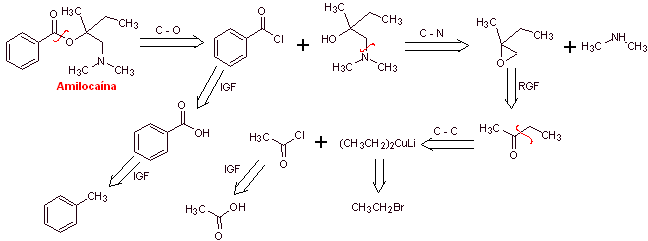
Síntesis de la amilocaína: La molécula precursora 2-butanona requerida,
puede ser preparada a partir del ácido acético y el reactivo de Gillman
correspondiente. Lo que lleva a preparar el epóxido a partir de la misma
cetona, utilizando el iluro de azufre respectivo, para introducir el grupo metileno (–CH2-).
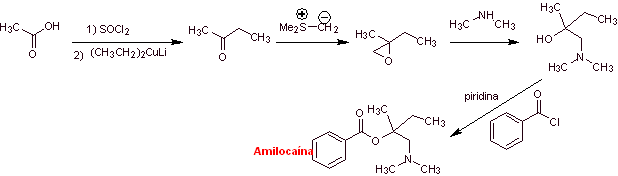
|
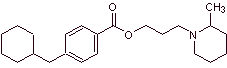
MOb 05: La ciclometicaína es otro
anestésico local importante. Proponer un plan de síntesis para este fármaco,
partiendo de materiales simples y asequibles. |
|
Análisis retrosintético: La desconexión se inicia por el enlace
acilo-oxígeno del grupo éster y luego se continúa con las desconexiones de las
dos moléculas precursoras generadas, hasta arribar al benceno, tolueno, cetona
y ácido acético como materiales de partida.
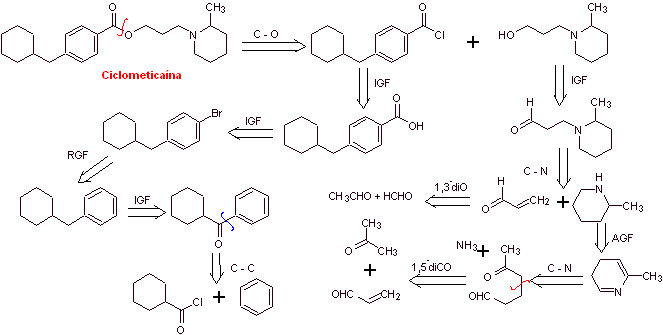
Síntesis de la ciclometicaína:
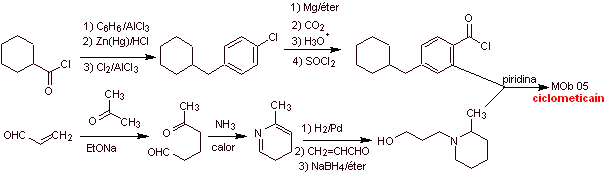
|
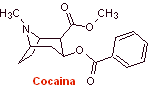
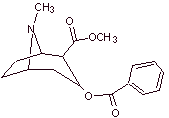
MOb 06: La
cocaína
es el primer anestésico local de origen natural, obtenido a partir de las
hojas de coca, y que lamentablemente se lo ha utilizado mayormente de manera
inescrupulosa por los efectos alucinógenos de la misma.
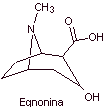
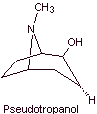
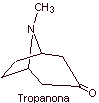
Pese a ello, se han obtenido
varios derivados de la cocaína, todos ellos utilizados como anestésicos
locales, como son por ejemplo, la ecgonina, |
|
|
|
… |
|
|
|
|
|
|
|
|
|
Con
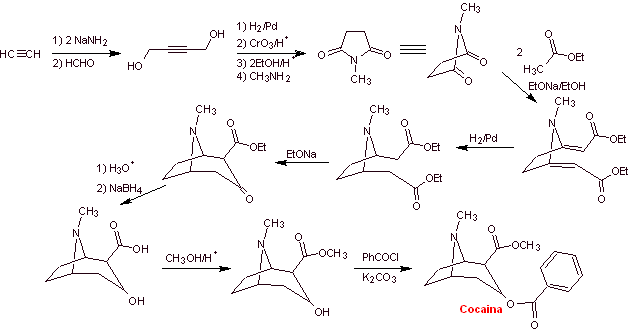
fines esencialmente médicos y terapéuticos, la cocaína ha sido sintetizada en
los laboratorios de química. Describir una posible ruta de síntesis química
para la cocaína a partir de materiales simples.
Análisis retrosintético: La desconexión se inicia por
enlace acilo oxígeno del éster unido directamente al compuesto bicíclico,
aspecto que simplifica bastante la estructura y forma moléculas precursoras,
mucho más fáciles de encarar en sus desconexiones. Luego se forma la egnonina, la misma que se desconecta por
una retro-condensación de Claisen, para continuar con una retro Knoevenagel.
Las posteriores desconexiones originan moléculas precursoras que llegan hasta
el acetileno y el formaldehído como materiales de partida.
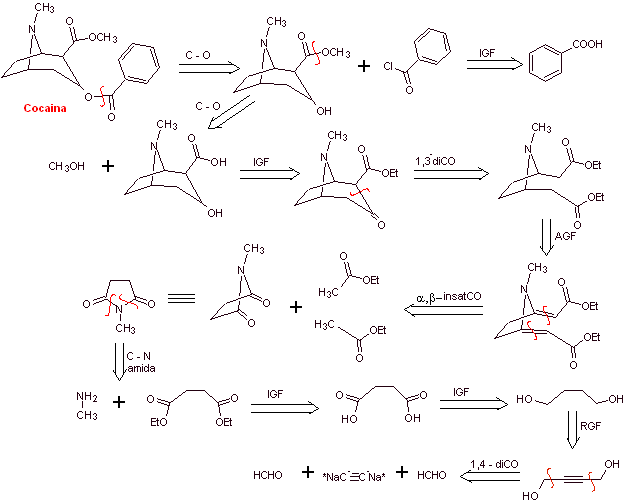
Síntesis de