Sintesi di isochinoline
(Con il metodo delle disconnessioni)
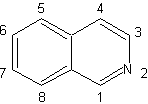
| Le isochinoline differiscono strutturalmente dalle chinoline nella posizione azoto, poiché quest'ultimo non è fuso, quindi presenta una "reattività alifatica". Non si trova libero in natura, ma il ciclo delle isochinoline si trova in alcuni alcaloidi, in forma aromatica o ridotta, ad esempio la papaverina. |
I metodi sintetici più noti per la preparazione delle isochinoline iniziano con 2-feniletilammine e comportano una ciclizzazione attraverso un carbonio aggiuntivo fornito dal gruppo carbonilico di un altro composto.
I principali metodi di sintesi sono: la sintesi di Pomeranz-Fritsch, la sintesi di Bischler-Napieralski, la sintesi di Pictet-Gams e la sintesi di Pictet-Spengler.
1. Sintesi di POMERANZ-FRITSCH.
Questo metodo di sintesi dell'isochinolina avviene in due fasi:
A.
Innanzitutto, la benzaldeide (1,3-elettrofilo-nucleofilo) viene condensata con amminoacetaldeide dietilacetale (1,3-nucleofilo-elettrofilo) per formare un'aldimina stabile.
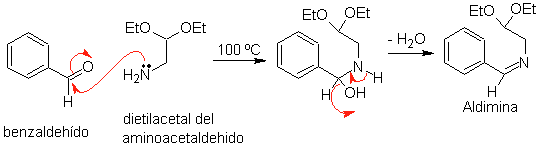
B.
Successivamente, l'aldimina ciclizza in un ambiente acido forte, ad un'immina, con contemporanea eliminazione dell'etanolo, per produrre un'isochinolina.
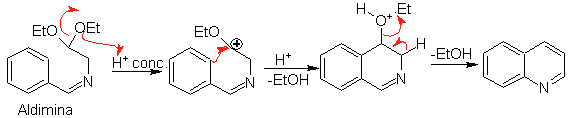
Questo secondo stadio, essendo una sostituzione elettrofila, è soggetto all'effetto che i sostituenti elettron-donatori o accettanti hanno sull'anello benzenico in detta reazione. Tuttavia, a causa dell'idrolisi dell'immina formata, nel mezzo acido forte utilizzato nella reazione, la resa del processo è ridotta.
Questo metodo consente l'accesso alle isochinoline C-1 sostituite, per le quali sono stati testati chetoni aromatici, con rese molto basse. Tuttavia, vi è stato un maggiore successo utilizzando la variante di benzilammine opportunamente sostituite come 1,4-dinucleofili e gliossale dietilacetale come 1,2-dielettrofili.
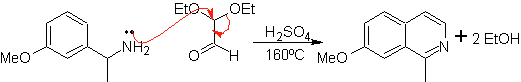
Una cosa che va chiarita è che il metodo Pomeranz-Fritsch e la sua variante, precedentemente analizzata, non consentono la preparazione di isochinoline sostituite in C-3 e C-4 dell'eteroatomo. L'analisi retrosintetica di questo metodo mostra i possibili intermedi coinvolti nella reazione ei probabili materiali di partenza.
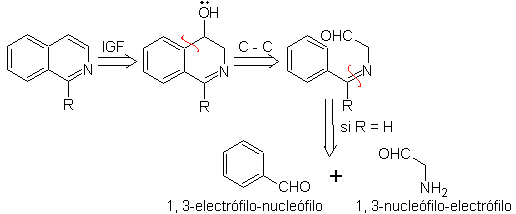
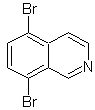
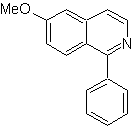
Proporre un progetto di sintesi per ciascuna delle seguenti isochinoline: | MOb 107
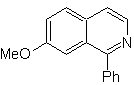
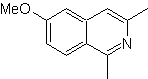
| MOb 108
|
MOb 107 . Analisi retrosintetica . La disconnessione di
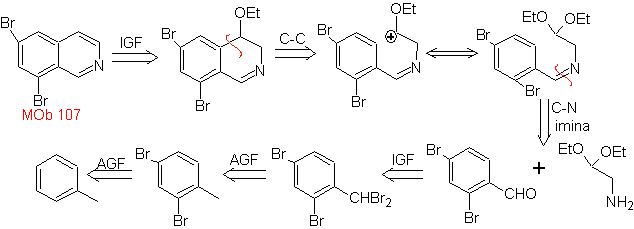
MOb 108. Analisi retrosintetica . La presenza di un sostituente su C1 di isochinolina, porta a disconnettersi
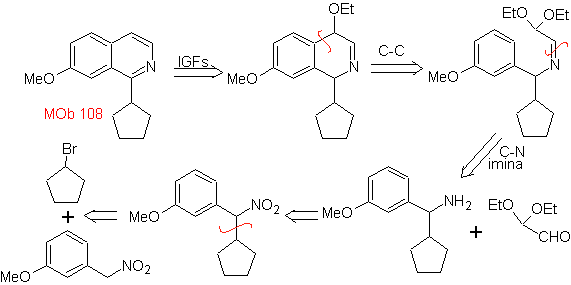
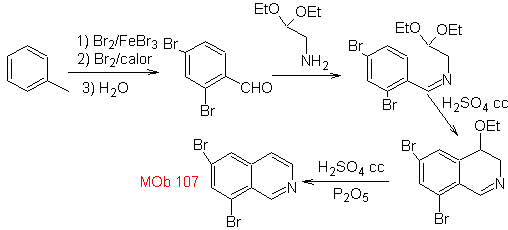
Sintesi Il derivato benzialminico viene preparato per reagire con l'aminoaldeide diacetale, secondo la sintesi di Pomeranz-Fritsch, per formare
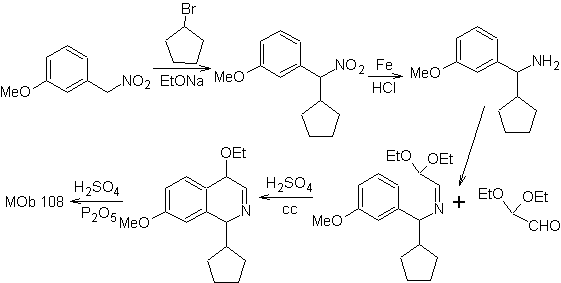
2. Sintesi BISCHLER-NAPIERALSKI .
Questo metodo sintetico delle isochinoline prevede la reazione di una fenetilammina (1,5-dinucleofila) con un cloruro o anidride acida (elettrofila) per formare un'ammide, la cui ciclizzazione con perdita di acqua porta a una 2,4-diidroisochinolina con un sostituente a C-1, che viene ossidato a isochinolina con Pd-C o fenil disolfuro.
La fase di ciclizzazione è una sostituzione aromatica elettrofila e quindi sarà favorita da sostituenti donatori di elettroni sull'anello aromatico della fenetilammina. Le fenetilamine m-sostituite portano esclusivamente a isochinoline C-6 sostituite, per ciclizzazione in posizione para rispetto al gruppo attivante.
L'analisi retrosintetica delle isochinoline preparate con questo metodo è la seguente:
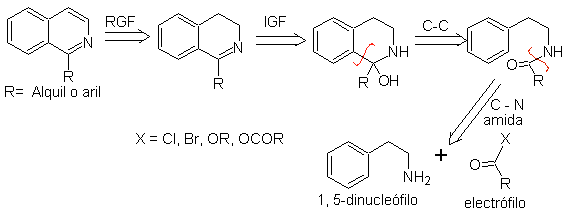
Gli agenti di ciclizzazione più frequentemente utilizzati in questa sintesi sono:
A.
P 2 O 5 (anidride fosforica)
B.
POCl 3 (ossicloruro di fosforo) e
C.
SOCl 2 (cloruro di tionile)
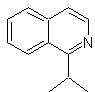
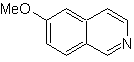
Proporre un piano di sintesi per le seguenti isochinoline: | MOb 109
| MOb 110
|
MOb 109 . Analisi retrosintetica .
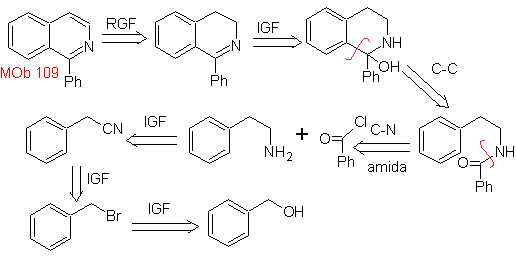
Sintesi. L'alcool benzilico è un buon materiale di partenza per formare la fenetilammina, che è combinata con il cloruro di benzoile. Il prodotto viene ciclizzato e aromatizzato con Pd/C e riscaldato per formare
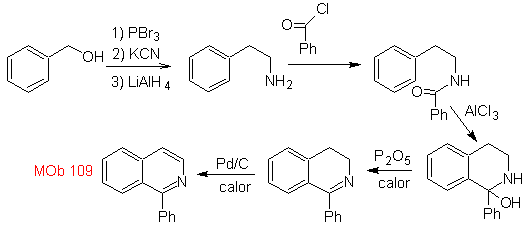
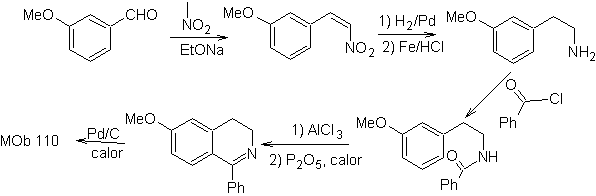
MOb 110. Analisi retrosintetica.
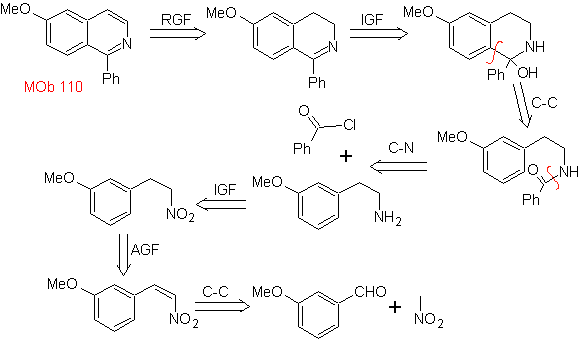
Sintesi. La sintesi di
3.
Sintesi PICTET-GAMS.
È una variante della sintesi di Bischler-Napieralski, in questo metodo si utilizzano fenetilamine potenzialmente insature ottenendo un eterociclo totalmente aromatico, quindi non è necessaria l'applicazione di ossidanti.
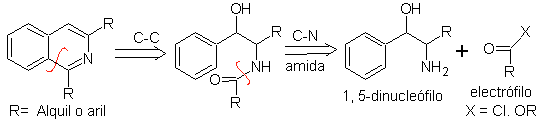
L'analisi retrosintetica di questo metodo mostra le seguenti potenziali riconnessioni e materiali di partenza.
Proporre un progetto di sintesi per la seguente isochinolina : | MOb 111.
|
MOb 111 . Analisi retrosintetica . Per avviare la disconnessione
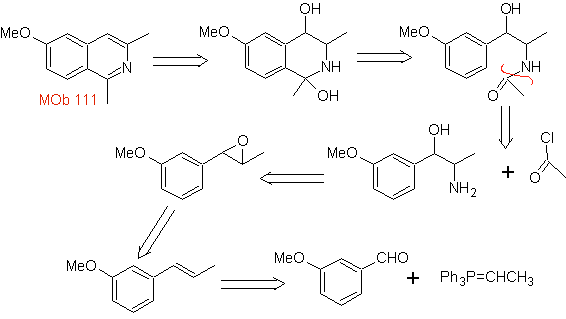
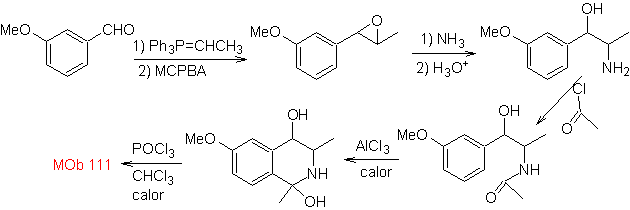
sintesi . Viene applicata la sintesi di Pictet-Gams, quindi non è necessario utilizzare un ossidante alla fine, per raggiungere la formazione di
Le fenetilamine possono anche reagire con le aldeidi con buone rese, dando aldimine che possono ciclizzare in ambiente acido a 1,2,3,4-tetraidroisochinoline, che devono essere ossidate per produrre isochinoline.
Questa ciclizzazione richiede sostituenti attivanti opportunamente posizionati per attivare le posizioni orto al gruppo amminoetile, motivo per cui la chiusura dell'anello avviene sempre in posizione para all'attivatore.
Quando l'anello aromatico è attivato con sostituenti idrossilici, la chiusura dell'anello avviene in condizioni molto blande, a causa del forte effetto attivante dell'OH-
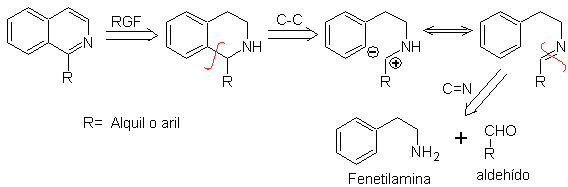
Analisi retrosintetica di un'isochinolina formata con il metodo Pictet-Spengler , mostra le seguenti disconnessioni e materiali di partenza:
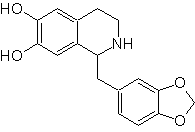
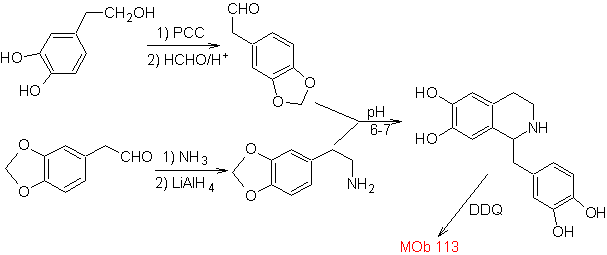
Proporre un piano di sintesi per le seguenti Isochinoline: | MOb 112
| ….. | MOb 113
|
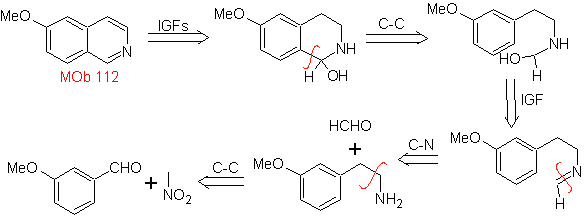
MOb 112. Analisi retrosintetica .
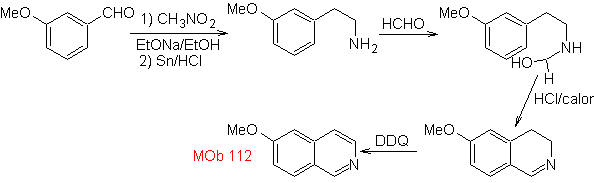
sintesi . La ciclizzazione avviene in ambiente acido e il DDG viene utilizzato per aromatizzare l'idroisochinolina formata per preparare
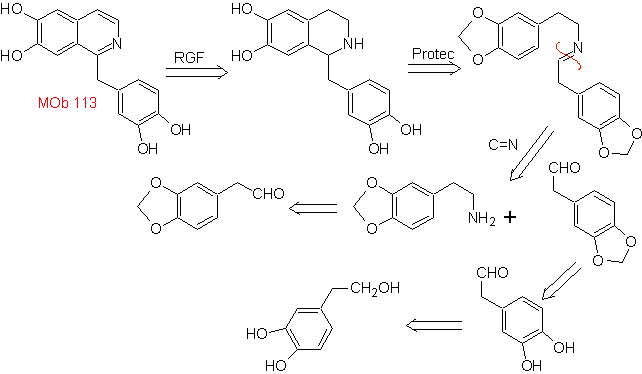
Sintesi La sintesi di Pictet-Spengler è applicata alla forma
Amé Pictet (1857-1937) era uno dei sei membri della rappresentanza svizzera e fungeva da segretario del Congresso della chimica di Ginevra . In qualità di rappresentante di