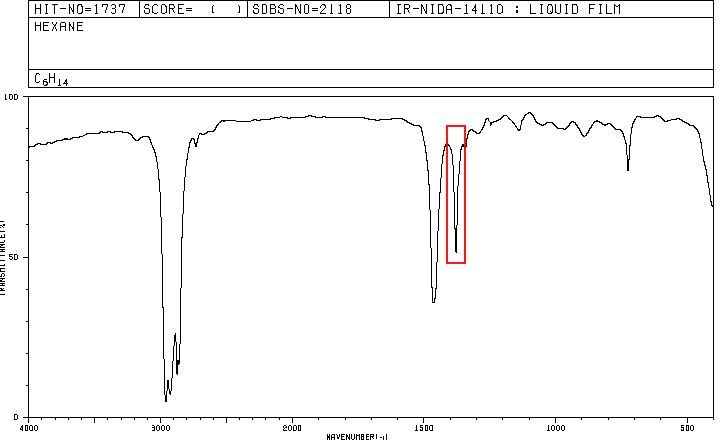
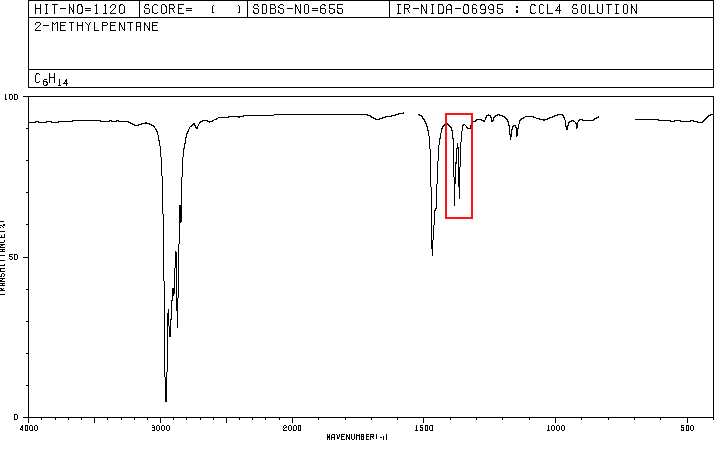
Eine organische Verbindung, deren prozentuale Zusammensetzung 83,63 % Kohlenstoff und 16,37 % Wasserstoff mit einer Molekülmasse von 86,11 beträgt, zeigt das folgende IR-Spektrum.
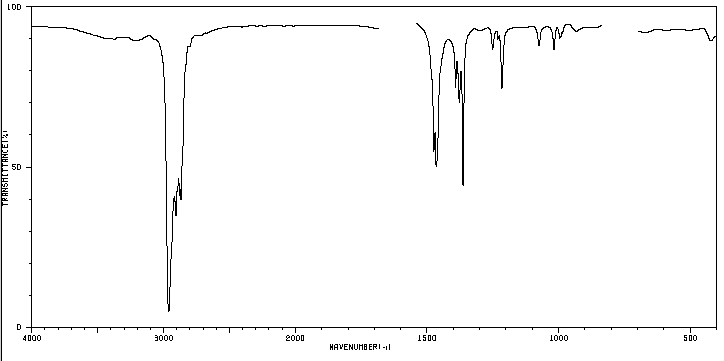
Bestimmen Sie die Struktur der Verbindung.
1. Bestimmung der Summenformel
\(C:\frac{83,63}{12,01}=6,96;\;\;\; H:\frac{16,37}{1,008}= 16,24\). Division durch den kleinsten Wert \(C:\frac{6.96}{6.96}=1;\;\;\;H:\frac{16.24}{6.96}=2.33\) . Durch Multiplizieren mit 3 erhalten wir ganzzahlige Werte C:3 H:7. Daher lautet die empirische Formel \((C_3H_7)_n\).
2. Bestimmung der Summenformel
\(n=\frac{86.11}{3\times 12.01+7\times 1.008}=2\). Die Summenformel lautet: C 6 H 14
3. Bestimmung des Ungesättigtheitsindex.
Beim Vergleich mit der Formel \(C_nH_{2n+2}\) wird beobachtet, dass das Alkan mit 6 Kohlenstoffatomen 14 Wasserstoffatome hat. Daher fehlen unserer Summenformel Ungesättigtheiten (Alkan).
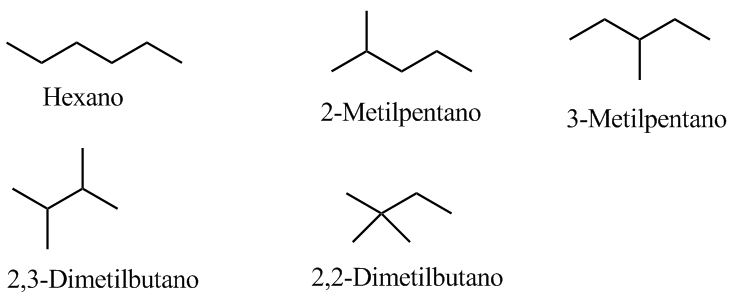
4. Schreiben Sie die möglichen Isomere auf.
Da es sich um eine gesättigte Verbindung handelt, enthält sie weder Zyklen noch Doppelbindungen.
5. Untersuchung des Spektrums, um zu bestimmen, zu welchem Isomer es gehört.
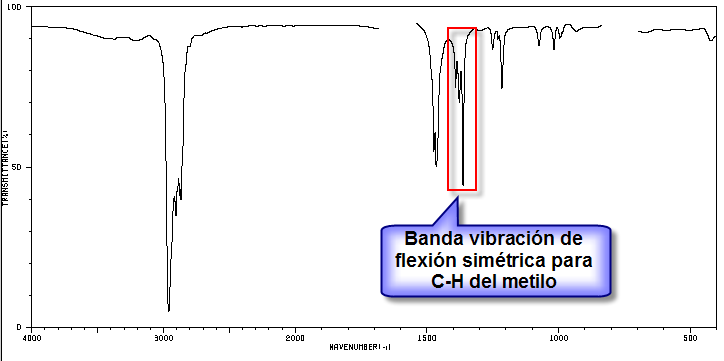
Die angezeigte Bande ist aufgrund der symmetrischen Biegeschwingung der Methyl-CH-Bindungen für die Isopropyl- und tert-Butylgruppen aufgespalten. Im Fall von Isopropyl erscheinen zwei Banden gleicher Intensität bei 1380 und 1370 cm –1 . Bei tert-Butyl hat die 1380-Bande die halbe Intensität. Wie in unserem Spektrum zu sehen ist, sind die beiden Banden unterschiedlich intensiv, was auf das Vorhandensein einer tert-Butylgruppe im Molekül hindeutet. Von den 5 vorgeschlagenen Isomeren stellt nur eines diese Gruppe dar, 2,2-Dimethylbutan.
Spektren für Hexan und 2-Methylpentan sind unten enthalten.