Les benzènes halogénés réagissent avec la soude diluée dans des conditions de pression et de température élevées pour former des phénols. Cette réaction ne nécessite pas de groupements désactivants en position ortho/para et suit un mécanisme différent de la substitution nucléophile aromatique par addition-élimination.
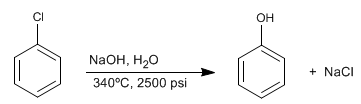
Cette réaction a été découverte en 1928 par des chimistes de la Dow Chemical Company. Le mécanisme consiste en l'élimination de HCl avec formation d'un intermédiaire instable appelé benzine, qui est attaqué par les ions hydroxydes du milieu, pour former du phénol.
Étape 1. Élimination du HCl
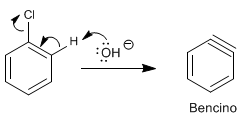
Étape 2. Ajout de l'ion hydroxyde à la benzine
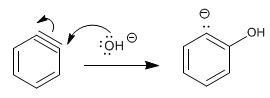
Étape 3. Protonation
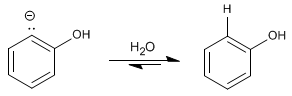
![]() Le mécanisme de cette réaction est appelé élimination-addition substitution nucléophile aromatique.
Le mécanisme de cette réaction est appelé élimination-addition substitution nucléophile aromatique.
Lorsqu'il y a des substituants dans le benzène, cela produit des mélanges, dus à l'attaque du nucléophile sur les deux carbones de la triple liaison.







