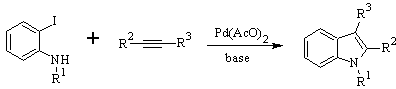Sintesis INDOLES
(Dengan metode pemutusan)
Sistem cincin indole telah ditemukan di banyak senyawa alami yang memiliki kepentingan kimia dan biokimia yang besar, oleh karena itu dikatakan paling melimpah di alam. Jadi, triptofan adalah asam amino esensial, nila adalah pewarna, dan asam indolil-3-asetat adalah hormon pertumbuhan tanaman. Di sisi lain, minat terhadap molekul ini muncul dari penggunaan farmakologisnya, contohnya sumatriptan (antimigrain) dan frovatriptan, juga antimigrain.
Indole adalah padatan kristal tidak berwarna dengan suhu mp 52°C, mudah larut dalam sebagian besar pelarut organik dan mengkristal dari air, memiliki bau yang menyenangkan dan karena itu juga digunakan sebagai bahan dasar parfum.
Ini pertama kali disiapkan pada tahun 1866 dengan memanaskan oxindole dengan debu seng dan telah menjadi produk komersial yang penting. Baeyer pada tahun 1869 mengusulkan sintesis berikut:
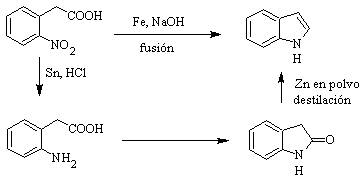
Metode sintesis klasik untuk indoles adalah dari Fischer, Bischler, Reissert dan Leimgruber-Batcho, Bartoli, Larock, Gassman, Sugasawa, Fukuyama, Hegedus, dan Dobbs.
1.
sintesis FISCHER
Ini terdiri dari pemanasan fenilhidrazon keton atau aldehida, dengan seng klorida anhidrat, boron trifluorida, asam polifosfat, atau beberapa katalis asam lainnya, untuk menghasilkan indol. Penataan ulang fenilhidrazon dengan katalis asam terjadi dengan eliminasi air dan NH 3 . Gugus elektrodonor mendukung siklisasi dan elektroatraktor menghalanginya.
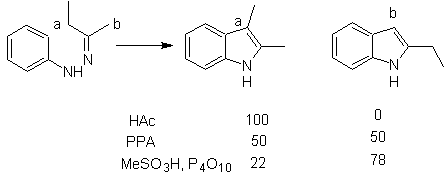
Dengan keton asimetris, siklisasi intramolekul hidrazon dapat menyebabkan dua indol isomerik dalam proporsi yang berbeda tergantung pada kondisi yang digunakan; dalam media yang sangat asam, indol yang kurang tersubstitusi dapat mendominasi.
Ketika ada substituen meta, sehubungan dengan nitrogen hidrazon, siklisasi dapat berlangsung di dua posisi, yang mengarah ke dua indol isomer:
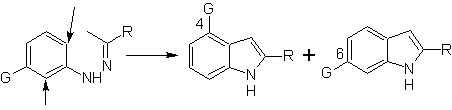
Jika substituen G adalah penarikan elektro, kedua isomer (4- dan 6-) terbentuk dengan perbandingan yang kira-kira sama. Di sisi lain, jika G adalah substituen penyumbang elektron, isomer tersubstitusi 6 terbentuk terutama.Analisis retrosintetik indol yang dibentuk oleh sintesis Fischer dapat dianggap sebagai berikut:
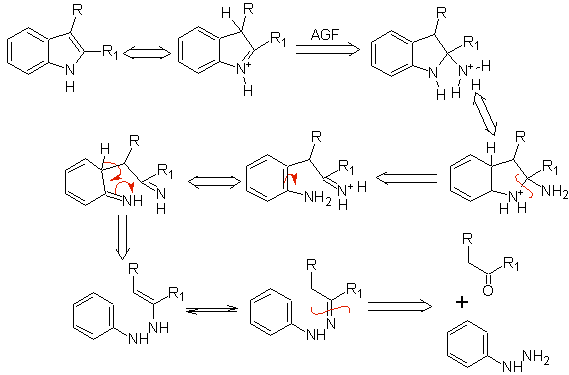
Usulkan rencana sintesis untuk molekul-molekul berikut: | MOb 119
| MOb 120
|
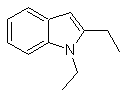
MOb 119. Analisis retrosintetik. Pemisahan mendasar dalam indol yang seharusnya dibentuk oleh sintesis Fischer sesuai dengan retro-transposisi, yang ditunjukkan dalam pemutusan
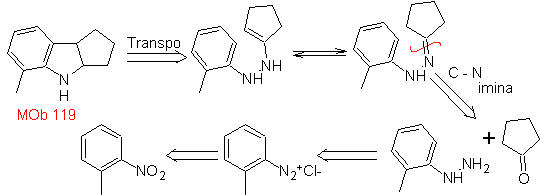
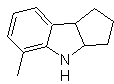
Sintesis : Dari orto-nitrotoluena, turunan antara fenilhidrazin dihasilkan, diperlukan dalam sintesis indol Fischer, imina dibentuk dengan siklopentanon, dan dengan pemanasan
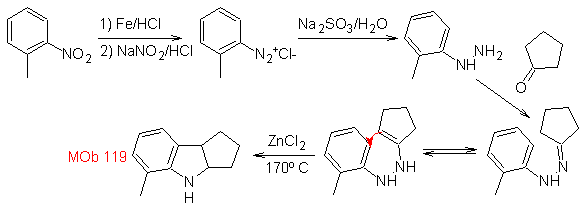
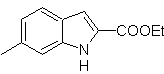
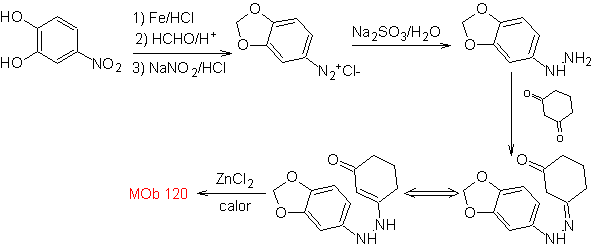
MOb 120. Analisis retrosintetik. Transposisi retro dari
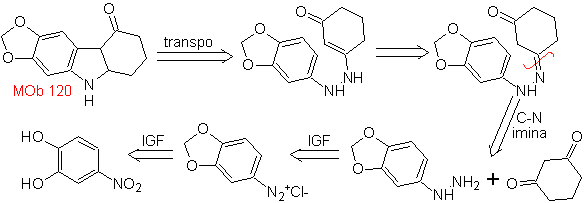
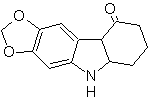
Perpaduan. OH dari molekul awal dilindungi, membentuk asetal siklik dan gugus nitro direduksi untuk kemudian diazotasikan amino.
Pengurangan senyawa diazo yang terbentuk dengan natrium sulfit, memungkinkan diperolehnya turunan fenilfidrazin, yang digabungkan dengan sikloheksanon, yang kemudian mengarah ke
1.
sintesis BISCHLER
Ini terdiri dari siklisasi yang dikatalisis asam dari α-arylaminoketone, yang dibuat dari anilin dan α-halocarbonyl. Menggunakan N-asilasi α-aminoketon, siklisasi lebih dapat dikontrol dan memungkinkan diperolehnya indola tersubstitusi dalam cincin heterosiklik
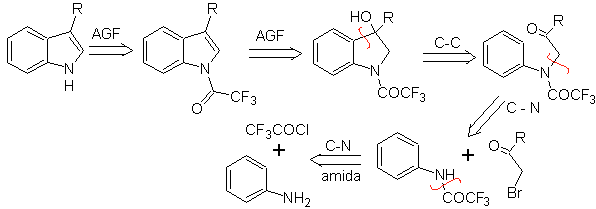
Usulkan desain sintesis untuk molekul-molekul berikut : | MOb 121
| MOb 122
|
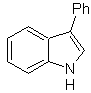
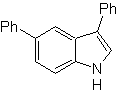
MOb 121 . Analisis retrosintetik.
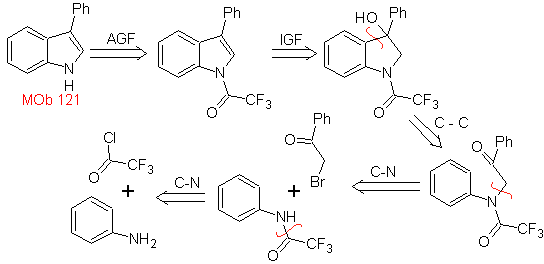
Perpaduan. Dimulai dari anilin, dapat diperoleh amida yang dibutuhkan, yang kemudian akan bereaksi dengan α-bromo benzofenon, membentuk molekul yang tersiklis dengan PPA. Penerapan basa seperti KOH dan panas, terbentuk
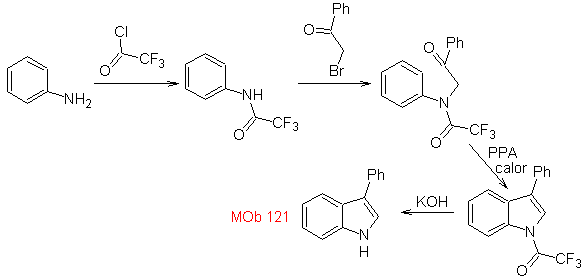
MOb 122 . Analisis retrosintetik.
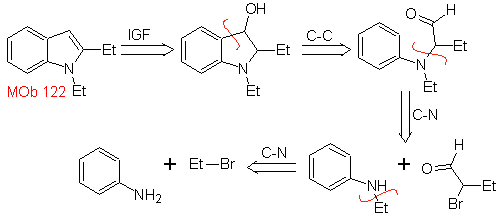
Perpaduan. Sekali lagi, sintesis dari
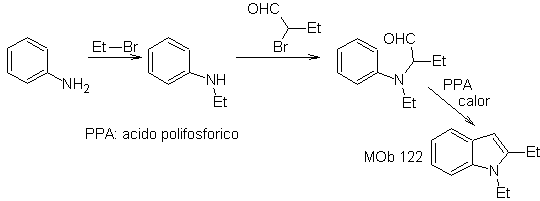
Dalam metode ini, hidrogen dari substituen pada posisi orto ke gugus nitro harus cukup asam, dan oleh karena itu nukleofil dijamin dalam pembentukannya, untuk bergabung dengan senyawa karbonil.
Usulkan rencana sintesis untuk molekul berikut: | MOb 123
| MOb 124
|
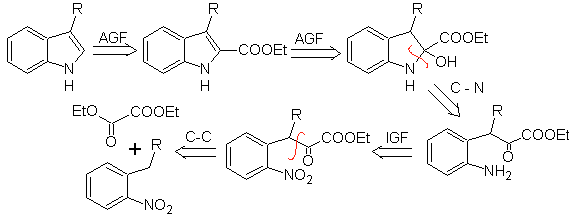
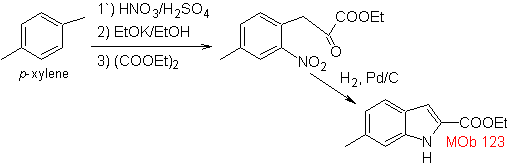
MOb 123 . Analisis retrosintetik.
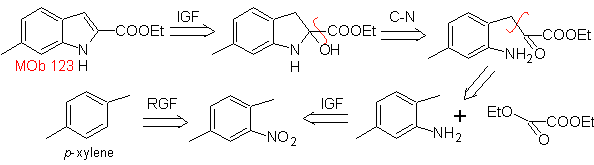
Perpaduan. p-xilena diubah menjadi turunan nitro, sebagai perantara yang diperlukan, untuk siklisasi, dekarboksilat dan dengan demikian terbentuk
MOb 124 . Analisis retrosintetik.
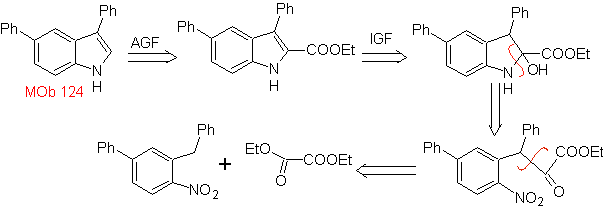
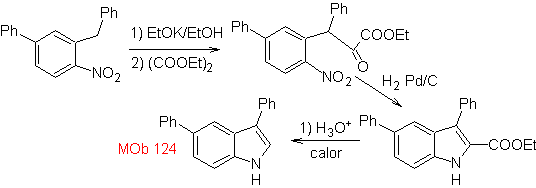
Perpaduan. Bahan awal yang diusulkan untuk sintesis
3.
Sintesis LEIMGRUBER-BATCHO
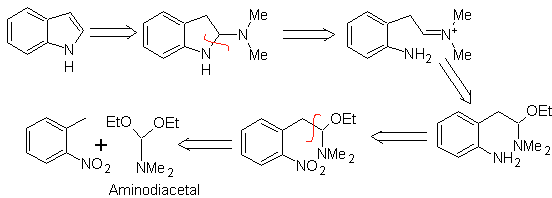
Seperti pada metode sebelumnya, keasaman substituen pada posisi orto ke gugus nitro harus dijamin, elektrofil yang dibutuhkan disediakan oleh aminodiasetal.
Usulkan rencana sintesis untuk molekul-molekul berikut: | MO 125
|
| MOb 126
|
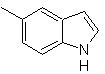
MOb 125. Analisis retrosintetik. Strategi pemutusan yang muncul dari sintesis Leimgruber-Batcho digunakan untuk
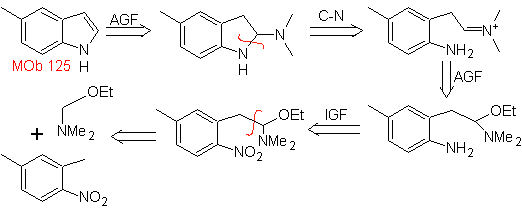
Perpaduan. Zat antara 2,4-dimetil-1-nitrobenzena dapat dibuat dari benzena dan dilanjutkan dengan reaksi yang disediakan dalam metode Leimgruber-Batcho, untuk sintesis
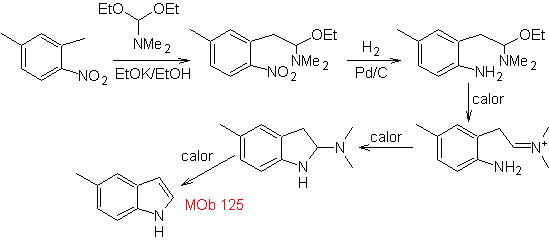
MOb 126 . Analisis retrosintetik. Gugus metil pada C2 dari indole memaksa pemutusan dihubungkan dengan adanya gugus asetilena, yang pada akhirnya akan bergabung dengan gugus amino.
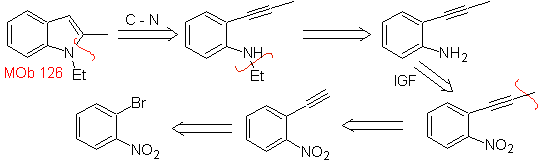
Perpaduan. Untuk memasukkan gugus asetilena ke dalam benzena, organomagnesium direaksikan dengan asetilena. Siklisasi dihasilkan oleh reaksi gugus amino dengan ikatan rangkap tiga. Reaksi berikut memungkinkan untuk terbentuk
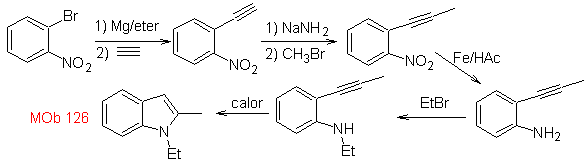
Sintesis HEGEDUS :
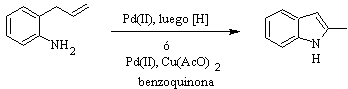
Sintesis FUKUYAMA :
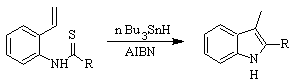
Sintesis SUGASAWA :
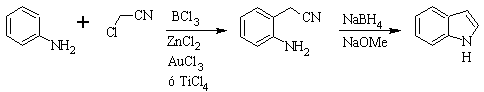
Sintesis Gassman :
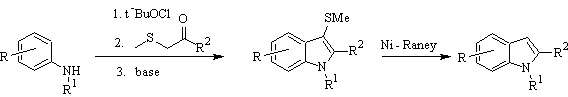
Sintesis BARTOLI:
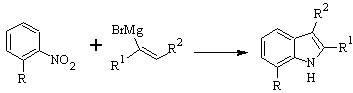
Sintesis DOBBS :
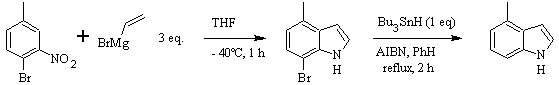
Sintesis CASTRO:
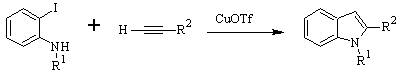
Sintesis LAROCK: