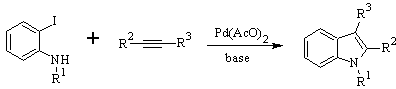Синтез ИНДОЛОВ
(методом разъединений)
Индольная кольцевая система была обнаружена во многих природных соединениях, представляющих большой химический и биохимический интерес, поэтому считается, что она наиболее распространена в природе. Так, триптофан — незаменимая аминокислота, индиго — краситель, а индолил-3-уксусная кислота — гормон роста растений. С другой стороны, интерес к этим молекулам возникает из-за их фармакологического применения, например, суматриптана (антимигренозного средства) и фроватриптана, также антимигренозного средства.
Индол — бесцветное кристаллическое вещество с т.пл. 52°С, легко растворимое в большинстве органических растворителей, кристаллизуется из воды, имеет приятный запах и поэтому также используется в качестве парфюмерной основы.
Впервые он был получен в 1866 году путем нагревания оксиндола с цинковой пылью и стал важным коммерческим продуктом. Байер в 1869 году предложил следующий синтез:
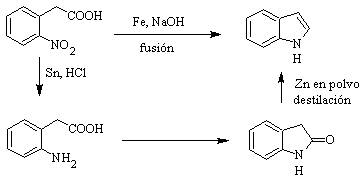
Классическими методами синтеза индолов являются методы Фишера, Бишлера, Рейссерта и Леймгрубер-Батчо, Бартоли, Ларок, Гассман, Сугасава, Фукуяма, Хегедус и Доббс.
1.
синтез Фишера
Он заключается в нагревании фенилгидразонов кетонов или альдегидов с безводным хлоридом цинка, трехфтористым бором, полифосфорной кислотой или каким-либо другим кислотным катализатором с получением индолов. Катализируемая кислотой перегруппировка фенилгидразона происходит с отщеплением воды и NH 3 . Электродонорные группы способствуют циклизации, а электроаттракторы препятствуют ей.
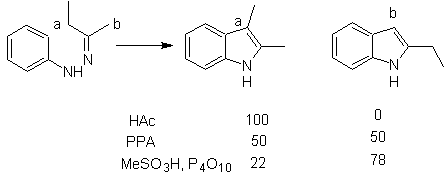
В случае асимметричных кетонов внутримолекулярная циклизация гидразона может приводить к двум изомерным индолам в различных соотношениях в зависимости от используемых условий, в сильнокислых средах может преобладать менее замещенный индол.
При наличии метазаместителей по отношению к азоту гидразона циклизация может происходить в двух положениях, что приводит к двум изомерным индолам:
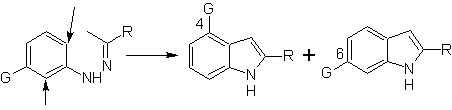
Если заместитель G электроакцепторный, то два изомера (4- и 6-) образуются примерно в одинаковой пропорции. С другой стороны, если G является электронодонорным заместителем, то в основном образуется 6-замещенный изомер.Ретросинтетический анализ индола, образующегося в результате синтеза Фишера, можно рассматривать следующим образом:
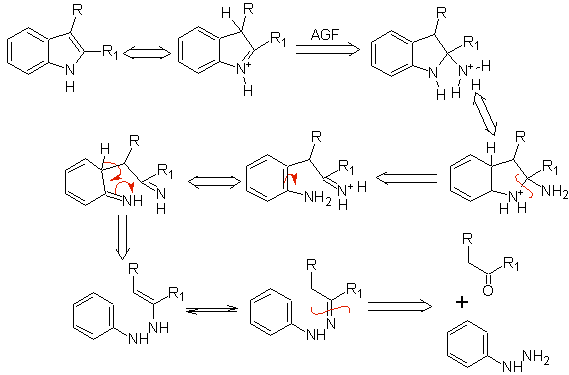
Предложите схему синтеза следующих молекул: | МОБ 119
| МОБ 120
|
MOb 119. Ретросинтетический анализ. Фундаментальное разъединение индолов, которые, как предполагается, образуются в результате синтеза Фишера, соответствует ретротранспозиции, которая проявляется в разъединении
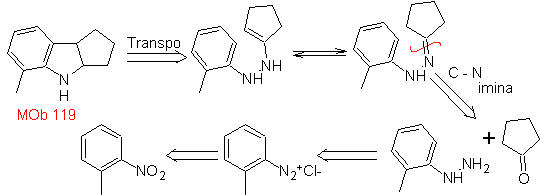
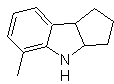
Синтез : из орто-нитротолуола образуется промежуточное производное фенилгидразина, необходимое для синтеза индолов Фишера, имин образуется с циклопентаноном, а при нагревании
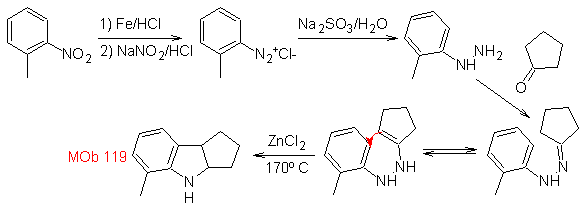
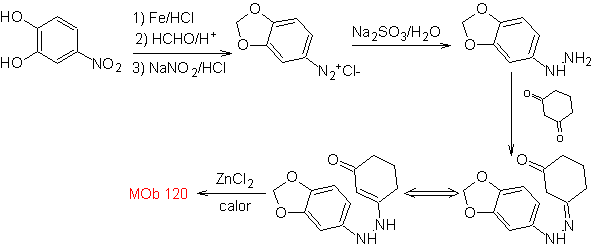
MOb 120. Ретросинтетический анализ. Ретро-транспозиция
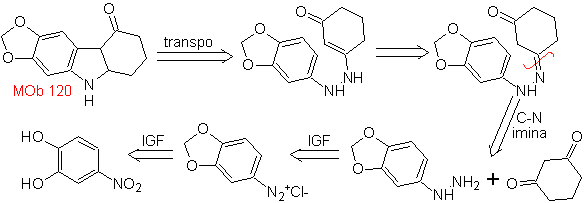
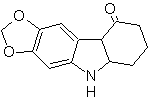
Синтез. ОН исходной молекулы защищается, образуя циклический ацеталь, а нитрогруппа восстанавливается для последующего диазотирования аминогруппы.
Восстановление образующегося диазосоединения сульфитом натрия позволяет получить производное фенилфидразина, которое соединяется с циклогексаноном, что затем приводит к
1.
синтез БИСХЛЕРА
Он состоит из катализируемой кислотой циклизации α-ариламинокетона, который получают из анилина и α-галогенкарбонила. При использовании N-ацилированных α-аминокетонов циклизация более контролируема и позволяет получать замещенные индолы в гетероциклическом кольце.
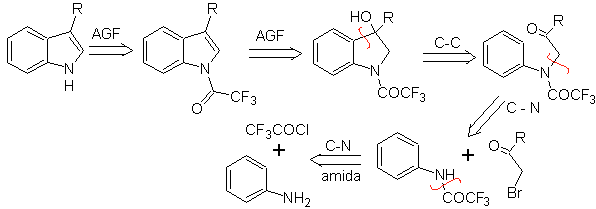
Предложите схему синтеза следующих молекул : | МОБ 121
| МОБ 122
|
МОБ 121 . Ретросинтетический анализ.
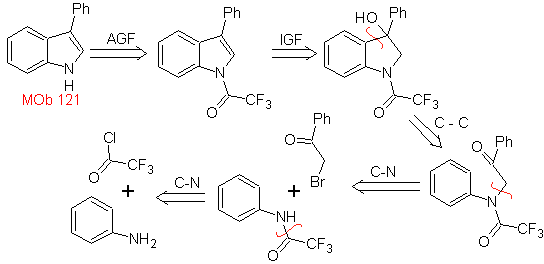
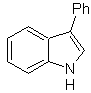
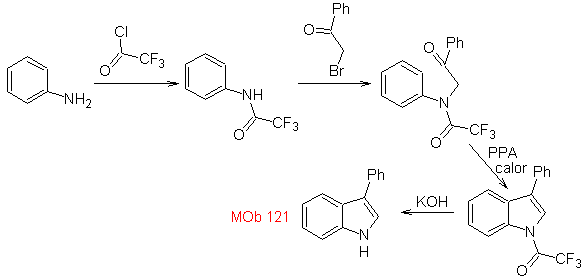
Синтез. Исходя из анилина, можно получить требуемый амид, который затем будет реагировать с α-бромбензофеноном с образованием молекулы, которая циклизуется с ПФК. Применение основания, такого как КОН, и нагревание образует
МОБ 122 . Ретросинтетический анализ.
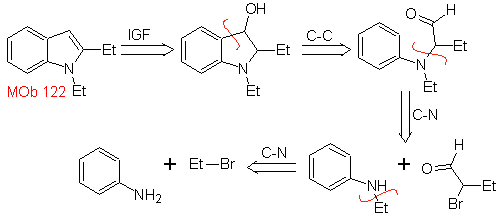
Синтез. И снова синтез
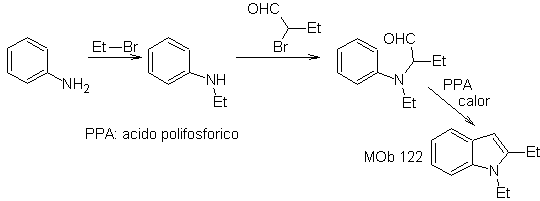
В этом методе важно, чтобы атомы водорода заместителя в орто-положении к нитрогруппе были достаточно кислыми, и поэтому нуклеофил гарантированно при его образовании соединяется с карбонильным соединением.
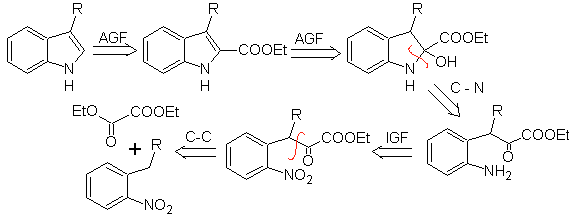
Предложите план синтеза для следующих молекул: | МОБ 123
| МОБ 124
|
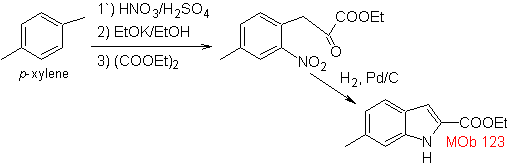
МОБ 123 . Ретросинтетический анализ.
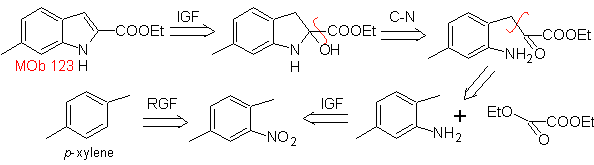
Синтез. п-ксилол превращается в нитропроизводное в качестве необходимого промежуточного продукта для циклизации, декарбоксилат и, таким образом, образуют
МОБ 124 . Ретросинтетический анализ.
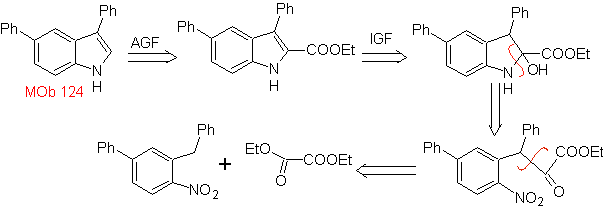
Синтез. Исходный материал, предлагаемый для синтеза
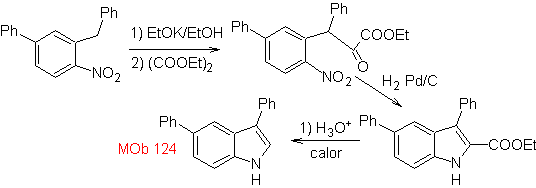
3.
Синтез ЛЕЙМГРУБЕРА-БАЧО
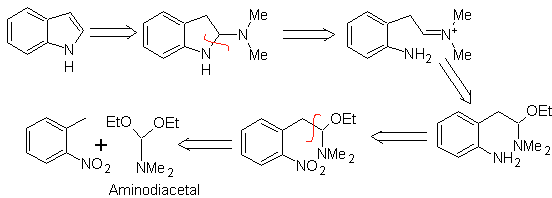
Как и в предыдущем методе, должна быть гарантирована кислотность заместителя в орто-положении к нитрогруппе, необходимый электрофил обеспечивается аминодиацеталем.
Предложите схему синтеза следующих молекул: | МОБ 125
|
| МОБ 126
|
MOb 125. Ретросинтетический анализ. Стратегия отключения, возникающая в результате синтеза Леймгрубера-Бачо, используется для
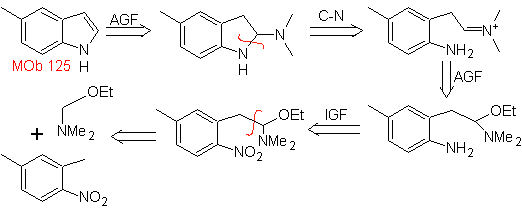
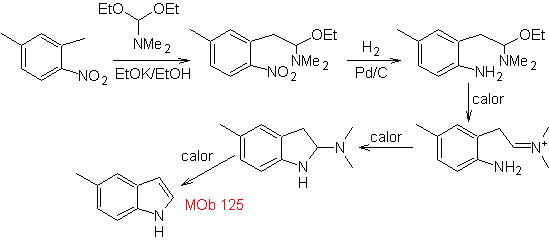
Синтез. Промежуточный продукт 2,4-диметил-1-нитробензол может быть получен из бензола и продолжен по реакциям, предусмотренным в методе Леймгрубера-Бачо, для синтеза
МОБ 126 . Ретросинтетический анализ. Метильная группа при С2 индола заставляет разрывы быть связанными с присутствием ацетиленовой группы, которая в конечном итоге соединится с аминогруппой.
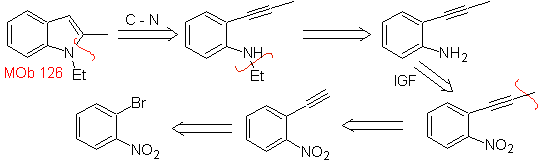
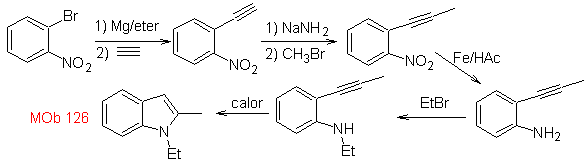
Синтез. Чтобы ввести ацетиленовую группу в бензол, магнийорганическое соединение взаимодействует с ацетиленом. Циклизация происходит в результате реакции аминогруппы с тройной связью. Следующие реакции позволяют получить
Синтез ГЕГЕДУС :
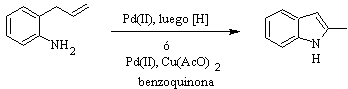
Синтез Фукуямы :
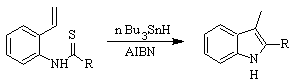
Синтез СУГАСАВА :
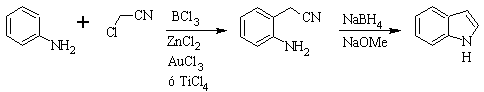
Синтез Гассмана :
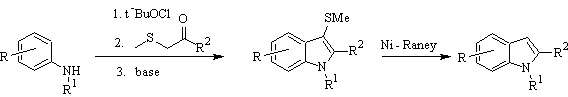
Синтез БАРТОЛИ:
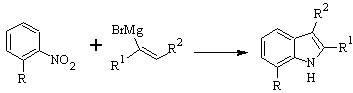
Синтез ДОББС :
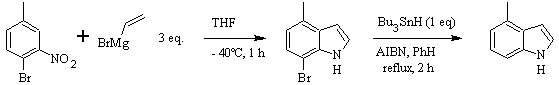
Синтез КАСТРО:
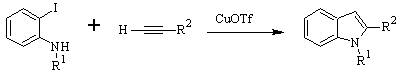
ЛАРОК Синтез: