Ciclização intramolecular (Williamson intramolecular): Álcoois halogenados na posição 2 ciclizam em meio básico para formar oxiranos.
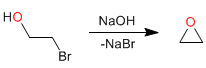
Mecanismo:
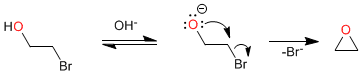
A primeira etapa do mecanismo consiste em um equilíbrio ácido-base que depotifica o álcool, gerando um bom nucleófilo (alcóxido) que cicliza na segunda etapa através de um S N 2 intramolecular.
Epoxidação de alceno: Perácidos (MCPBA) reagem com alcenos para formar oxiranos (epóxidos).

Mecanismo:
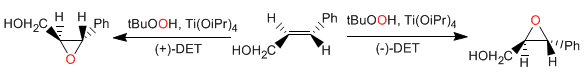
Epoxidação assimétrica de Sharples: Álcoois alílicos reagem enantiosseletivamente com tetraisopropóxido de titânio, terc-butilhidroperóxido e (+) ou (-) dietiltartarato para dar oxiranos.
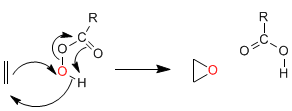
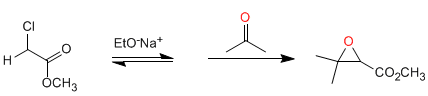
Síntese de Darzens: A reação começa a partir de ésteres halogenados em posição alfa, que formam enolatos em meio básico. A reação do éster enolato com aldeídos ou cetonas, seguida de S N 2 intramolecular, produz oxiranos.
Mecanismo:
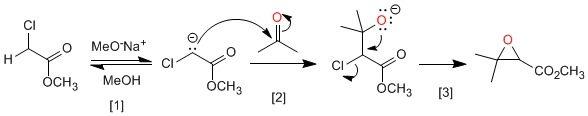
[1] Desprotonação do éster.
[2] Ataque nucleofílico do éster enolato na carbonila.
[3] Substituição nucleofílica intramolecular que gera oxirano.
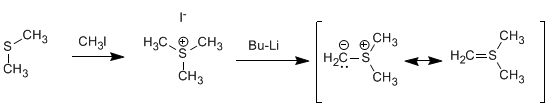
Síntese de núcleo (iletos de enxofre): Iletos de enxofre reagem com aldeídos ou cetonas para formar oxiranos.
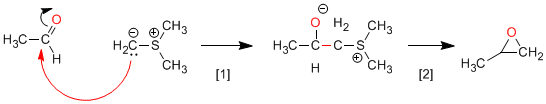
[1] Ataque nucleofílico do ilídeo ao carbonil.
[2] Estágio de ciclização aproveitando a capacidade do enxofre como grupo abandonador.
O ileto de enxofre é preparado pela metilação do sulfeto de dimetila seguido de tratamento com base forte.