Ciclizzazione intramolecolare (Williamson intramolecular): gli alcoli alogenati in posizione 2 ciclizzano in mezzi basici per formare ossirani. 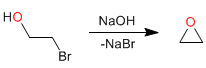
Meccanismo: 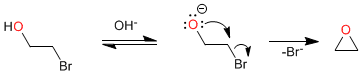
Il primo stadio del meccanismo consiste in un equilibrio acido-base che depotizza l'alcool, generando un buon nucleofilo (alcossido) che ciclizza nel secondo stadio attraverso un S N 2 intramolecolare.
Epossidazione degli alcheni: i peracidi (MCPBA) reagiscono con gli alcheni per formare ossirani (epossidi). 
Meccanismo: 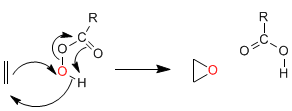
Epossidazione asimmetrica di Sharples: gli alcoli allilici reagiscono enantioselettivamente con titanio tetraisopropossido, terz-butilidroperossido e (+) o (-) dietiltartrato per dare ossirani. 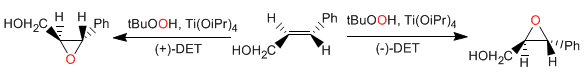
Sintesi di Darzens: la reazione inizia da esteri alogenati in posizione alfa, che formano enolati in un mezzo basico. La reazione dell'estere enolato con aldeidi o chetoni, seguita da S N 2 intramolecolare, produce ossirani. 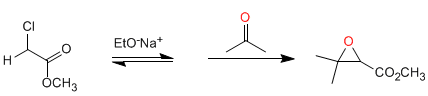
Meccanismo: 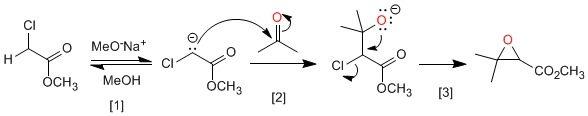
[1] Deprotonazione dell'estere.
[2] Attacco nucleofilo dell'estere enolato sul carbonile.
[3] Sostituzione nucleofila intramolecolare che genera ossirano.
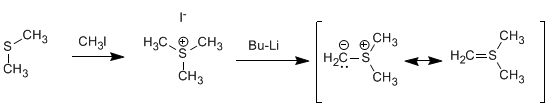
Sintesi di Corey (ilidi di zolfo): le ilidi di zolfo reagiscono con aldeidi o chetoni per formare ossirani. 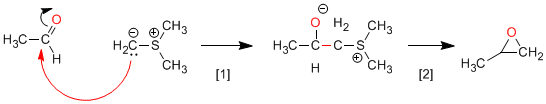
[1] Attacco nucleofilo dell'ilide al carbonile.
[2] Fase di ciclizzazione che sfrutta la capacità dello zolfo come gruppo uscente.
L'ilide di zolfo viene preparata mediante metilazione del dimetil solfuro seguita da trattamento con base forte.